Сайт учителя хімії Видай Олени Василівни
|
Статистика
Онлайн всього: 1 Гостей: 1 Користувачів: 0 |
Атоми і хімічні елементи. Молекули. Рух молекул. Дифузія
Тема уроку: "Атоми і хімічні елементи. Молекули. Рух молекул. Дифузія»
Мета уроку: сформувати в учнів поняття про атоми й молекули як складні структурні частинки речовини; дати уявлення про атомну та молекулярну будову речовини, рух молекул, дифузію; на підставі будови атома пояснити поняття хімічного елемента як виду атомів; ознайомити учнів із символами й назвами хімічних елементів за сучасною українською номенклатурою; сформувати уявлення про структуру Періодичної системи; дати уявлення про поширеність хімічних елементів у природі. Очікувані результати: учні мають уміти характеризувати частинки (атоми та молекули), з яких побудовані речовини; уміти характеризувати хімічний елемент як певний вид атомів; називати хімічні елементи за сучасною українською номенклатурою; записувати символи хімічних елементів; отримувати з Періодичної системи інформацію про хімічний елемент (назва, символ, порядковий номер, положення в періоді й групі). Базові поняття й терміни: атом, молекула, хімічний елемент, хімічні символи, Періодична система хімічних елементів Д. І. Менделєєва, період, група, порядковий номер, дифузія. Обладнання: хімічні склянки, прилад для нагрівання, вода, пакетики з чаєм, пластилін різних кольорів. Тип уроку: вивчення нового матеріалу. 1. Організаційний етап 1.1. Привітання. 1.2. Перевірка присутності учнів: кількість за списком _______, кількість присутніх на уроці ________, відсутніх ________. 1.3. Перевірка готовності учнів до уроку. 2. Етап перевірки домашнього завдання 2.1. Перевірка наявності в учнів виконаних письмових робіт. Обговорення питань, які виявилися найбільш складними. 2.2 Робота в зошитах Випишіть у два стовпчики назви тіл і речовин Склянка, ніж, алюміній, цвях, дріт, мідь, цукор ІІ варіант Залізні ошурки, залізо, кусок мила, вода, парафінова свічка, скло, скляна паличка 2.3 Поміркуймо разом За якими ознаками можна розпізнати речовини (мідь, алюміній, крейда, мармур, вода, олія)? 3. Актуалізація опорних знань і мотивація навчальної діяльності 3.1 Бліцопитування
3.2 Показ практичного значення вивчення нового матеріалу. Слово вчителя Люди здавна здогадувалися про те, що речовини складаються з окремих дрібних частинок. Ці елементи називають атомами. Зазвичай атоми не існують поодинці, а об’єднуються в більші утворення — молекули. Атоми й молекули надзвичайно малі: у будь-якому крихітному шматочку речовини, який ми здатні розгледіти (наприклад, у порошинці) міститься більше атомів, аніж зірок у всій нашій Галактиці. 3.3. Повідомлення теми уроку. 3.4. Формулювання разом з учнями мети й завдань уроку. 4. Етап засвоєння нових знань План пояснення нового матеріалу
Усі речовини складаються з найменших частинок — атомів. Той факт, що все, що нас оточує, складається з частинок, знали ще давні греки. Близько 420 р. до н. е. грецький філософ Демокрит висунув гіпотезу, що матерія складається з малесеньких неподільних частинок і запропонував називати їх атомами (тобто у перекладі з грецької ¾ неподільними). Деякі вчені продовжували дотримуватися думки, що матерія складається з атомів, але тільки на початку XIX ст. було отримано експериментальні дані, які підтвердили цю теорію. Англійський хімік Дж. Дальтон проводив досліди з газами й вивчав шляхи їх поєднання. Так, він виявив, що кисень і водень, утворюючи воду, завжди з’єднуються в тих самих пропорціях за масою. Він зробив висновок, що речовини складаються з атомів і що всі атоми простої речовини мають однакову масу. Отже, атом - це будівельний матеріал речовин, найдрібніша, хімічно неподільна частинка речовини. Речовини, які складаються з атомів називають речовинами атомної будови.
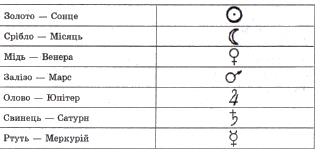
Нині відомо 118 видів атомів, тобто хімічних елементів. Із них у природі виявлено 89, решту отримано штучно. З різноманітної комбінації хімічних елементів складається понад 12 млн відомих нині речовин. Атоми різних видів відрізняються за масою і розмірами. Досить часто, розглядаючи поняття «хімічний елемент», проводять аналогію з літерами алфавіту: як із літер у різних комбінаціях можна скласти різні слова, так і з різних атомів з’єднань хімічних елементів постають різноманітні речовини. Ми й усе, що нас оточує, «зроблені» з хімічних елементів. Поет С. Щипачов у вірші «Читаючи Менделєєва» відзначив: Природа має лиш один секрет — Чи тут, чи там, у Космосу глибинах, Все: від малих піщинок до планет — Із елементів складене єдиних. За часів алхімії було відомо лише сім металів. І за збігом астрономи на той час якраз відкрили рівно сім планет. Алхіміки вирішили, що це не просто збіг! Вони ототожнили кожен метал із небесним світилом, відповідно надавши металам певні графічні позначення:
Та з плином часу відкривали все нові метали, і згодом відомих світил для того, аби називати їх, уже не вистачало. У 1814 р. шведський хімік Є. Я. Берцеліус запропонував позначати хімічні елементи однією або двома першими літерами з їхніх латинських назв. Наприклад: Оксиген позначають літерою О — від Oxygenium, Сульфур — S від Sulfur, Ферум — Fe від Ferrum тощо. Увага! Назви хімічних елементів завжди слід писати з великої літери. Усі відкриті на сьогодні хімічні елементи класифіковано у вигляді складної таблиці — Періодичної системи хімічних елементів Д. І. Менделєєва. Вона складається з горизонтальних періодів (їх сім) і вертикальних груп (їх вісім). Отже, хімічні елементи – це атоми одного виду, мають однакову будову, незалежно від того, до складу якої речовини вони входять. Кожен хімічний елемент має свою назву і письмове позначення, яке називають хімічним символом.
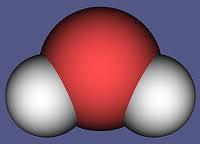
Усі речовини складаються з окремих частинок — молекул (від латин. moles — шматок). Молекулою називають найменшу частинку речовини, що має основні хімічні властивості цієї речовини й складається з атомів. Наприклад, найменша частинка води — молекула води, найменша частинка цукру — молекула цукру. Спробуймо уявити собі, якими є розміри молекул. Якби можна було скласти в один ряд впритул одна до одної 107 молекул води, то вийшла б нитка завдовжки лише 2 мм. Через дуже малі розміри молекули невидимі для неозброєного ока й навіть у прості оптичні мікроскопи. Але за допомогою спеціального приладу — електронного мікроскопа — науковцям удалося навіть сфотографувати найбільші з них. Так, науковці за допомогою дослідів довели, що молекули різних речовин відрізняються одна від одної, а молекули однієї речовини є однаковими. Наприклад, воду, отриману із соку або молока, не можна відрізнити від прісної води, отриманої шляхом перегонки з морської. Молекули води однакові. Молекули прийнято зображати схематично, тобто за допомогою моделей. Зображення молекули води:
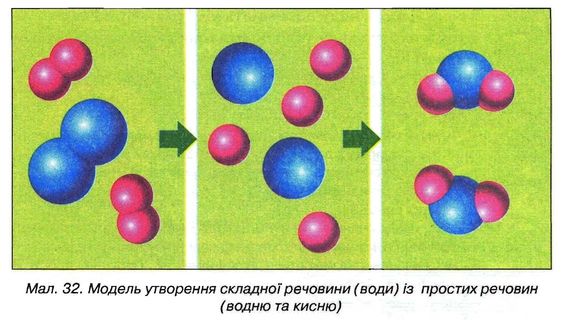
Молекули складаються з іще дрібніших частинок — атомів. Наприклад, найменша частинка води — це молекула води. Вона складається з трьох атомів: двох атомів Гідрогену й одного атома Оксигену. (Учням пропонується з пластиліну різних кольорів виліпити модель молекули води, а також за підказкою учителя моделі молекул інших речовин )
Молекули перебувають у безперервному русі. При зміні агрегатного стану речовини, змінюється взаємодія між молекулами.
Дифузія – це явище проникнення молекул однієї речовини між молекулами іншої. Дослід «Дифузія в рідинах». 1. Завдання для спостереження: а) зміна забарвлення води в склянках після опускання пакетиків чаю. б) швидкість забарвлення води у склянці з холодною та гарячою водою. 2. Проведення досліду і висновки. В склянки з холодною та гарячою водою одночасно опускаються пакетики з чаєм. Бесіда.
Молекули речовин, що входять до складу чаю, рухаючись безладно і хаотично, проникають між молекулами води і забарвлюють її. В гарячій воді молекули рухаються швидше, тому вона швидше забарвлюється.
Щось не хочеться сидіти. 6. Узагальнення й систематизація знань 6.1 Бесіда
6.2 Розгадати кросворд
6.3 Завдання Пояснити, в яких випадках йдеться про алюміній як про хімічний елемент, а в яких – як про просту речовину: а) глина містять алюміній; б) для виробництва алюмінію необхідна електрична енергія; в) за розповсюдження у природі алюміній посідає третє місце; г) алюміній використовують в літакобудуванні 6.4 Прийом «Третій зайвий» Учитель зачитує поняття, а учні визначають, яке з них є зайвим, і пояснюють свій вибір. 1. Сульфур, Нітроген, кисень. (Сульфур та Нітроген — хімічні елементи, кисень — речовина.) 2. Протони, нейтрони, Гідроген. (Протони й нейтрони — нуклони ядра, а Гідроген — хімічний елемент.) 3. Оксиген, водень, Гідроген. (Оксиген і Гідроген — хімічні елементи, водень — речовина.) 4. Аурум, молоко, повітря. (Повітря й молоко — суміші, Аурум — хімічний елемент.) 5. Гелій, Натрій, молоко. (Гелій та Натрій — хімічні елементи, молоко — суміш.) 6.5 Робота в парах Учні мають заповнити порожні клітинки в таблиці.
6. Домашнє завдання, інструктаж щодо його виконання Вивчити § 6 підручника Коршевнюк Т.В., Баштовий В.І., за заг. ред. Ярошенко О.Г. Природознавство. Виконати завдання після параграфів с. 31 7. Підбиття підсумків уроку Учитель пропонує учням висловитися щодо досягнення мети уроку. |
Пошук
Календар
Архів записів
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||